 红宝石hbs最新网站hbs123临床试验工作指引
红宝石hbs最新网站hbs123临床试验工作指引
机构办公室
2022年 03月
目录
1、项目立项
2、伦理审查
3、合同管理
4、项目启动
5、项目实施
6、项目结束
7、说明
临床试验工作指引
为帮助各科室、申办方及CRO熟悉本院药物/医疗器械临床试验机构的办事流程,更规范、流畅的开展临床试验,特编写本工作指引,供各方参考。
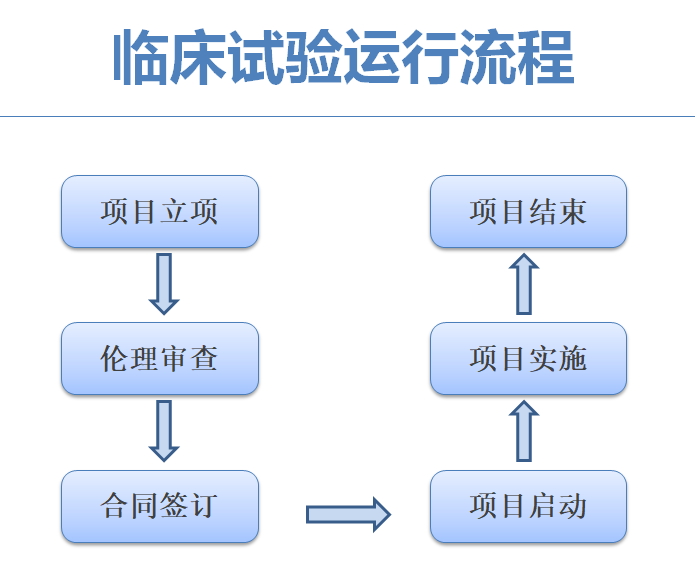
1 项目立项
1.1 科室/申办方/CRO通过电话/邮箱与药物/医疗器械临床试验机构办公室沟通,按机构办要求将电子版立项资料发至机构办邮箱,电子版立项资料审查无误后提交纸质版盖章立项资料。
1.2 机构办公室联系方式
联系人:吴巧稚、张婷婷
联系电话:025-89699088(外线),81021(内线) Email:jshjgb@126.com
地址:南京市鼓楼区江苏路65号3号楼4楼403室
1.3 立项资料提交后请尽快支付立项审查费(该费用涵盖项目前期接洽、立项前沟通、立项审核、立项资料档案管理、合同审议、合同费用估算、合同签批、启动会筹备等项目启动前事宜),并将转账凭证发送至机构办邮箱,转账凭证是立项审查的前提条件。
1.4 机构办公室对项目资料进行形式审查,依据项目具体情况确定是否需由学术委员会对项目进行实质性内容审查,形式审查常规情况下需要5个工作日,对需要实质内容审查的项目,立项审查时间会延长。立项审查合格者机构办书面通知伦理委员会,未接到书面通知的项目伦理委员会不予受理。机构办秘书将通过电话/邮件通知科室/申办方/CRO立项审查结果。
1
1.2
2 伦理审查
2.1 科室/申办方/CRO在收到机构立项通知后,可直接与伦理办公室联系,沟通伦理会议审查事宜。
2.2 伦理办公室联系方式
联系人:赵静
联系电话:025-89699426(外线),83158(内线) Email:jsslnyyjyk@126.com
地址:南京市鼓楼区江苏路65号3号楼4楼404室
2.3 科室/申办方/CRO需按照伦理办公室要求提交纸质版和电子版资料,收到伦理审查会议通知后,请尽快支付伦理审查费,并将转账凭证发送至伦理办公室邮箱,转账凭证是伦理委员会会议审查的前提条件。
2.4 根据审查项目数量的实际情况,伦理委员常规每月开会1次。对正式受理的申请项目,一般情况下伦理委员会在1个月内审查,审查决定在伦理会议5个工作日后告知科室/申办方/CRO和机构办。
2.5 项目研究进行期间,有如下情况需报伦理进行持续审查:
l 试验方案、知情同意书、招募材料等文件的修正
l 变更主要研究者
l SAE报告
l 不依从/违反研究方案
l 年度/定期跟踪审查
l 研究项目的暂停/终止
l 结题申请
3 合同管理
3.1 合同草稿
3.1.1 获得伦理委员会批件,同意开展临床试验的项目方可进行合同洽谈。
3.1.2 合同预算包括但不限于:研究者观察费、受试者补贴、受试者医疗开支、医院管理费、药物管理费、质控费、税费等。
3.2 合同审批
3.2.1 合同经各方审核达成共识后定稿。
3.2.2 如有CRO,需签订申办方、CRO和机构的三方协议。
3.2.3 如聘请CRC,需签订申办方/CRO、SMO和机构的三方协议。
3.2.4 签字盖章后的主合同交主要研究者签字后按照医院会签流程办理合同审批手续。
3.3 合同生效
3.3.1 合同生效后,申办方/CRO应按照合同约定及时拨付研究经费,银行汇款时需简要注明项目名称和费用用途,同时将银行转账凭证发至机构办公室邮箱jshjgb@126.com。
3.3.2 我院财务部门确认经费到帐后方可开具相应金额增值税普通发票。发票原则上不予邮寄,需由申办方/CRO工作人员到财务科签字领取,遗失不补。
3.4 合同关闭
试验结束后,由双方依据合同约定,共同核实试验项目费用,申办方/CRO支付合同尾款。
4 项目启动
4.1 监查员(CRA)
4.1.1 申办方/CRO需指定项目的监查员,保证监查员资质符合法规要求。
4.1.2 监查员需提供以下资料至机构办备案:
l 派遣函(盖公章)及简历
l 身份证复印件
l GCP培训证书及学历证书复印件
4.2 临床研究协调员(CRC)
4.2.1 临床研究协调员可由申办方/CRO 指定合格的 SMO 派遣,相关费用由申办方/CRO 支付。
4.2.2 派遣至我院独立工作的CRC需提供以下资料至机构办备案:
l 派遣函(盖公章)及简历
l 身份证复印件
l GCP培训证书及学历证书复印件
l 试验相关培训记录
l 公司营业执照
4.2.3 CRC需签订保密协议,仅限从事主要研究者授权下非医学性判断的相关事务性工作。CRC需定期向机构办公室汇报项目的进展情况。机构办可协助CRC办理临时工卡、就餐卡、工作服等手续,费用需自理。
4.3 物资交接
物资主要包含:项目文件资料、试验用药物、试验用医疗器械(包括体外诊断试剂)等。
4.3.1 项目文件资料
4.3.1.1 项目文件资料包括但不限于:试验方案、知情同意书、研究病历、病例报告表、随机编码表等。
4.3.1.2 申办方/CRO监查员与科室资料管理员提前联系,完成项目文件资料交接并签名确认。若通过快递方式交接的,需提供已签名确认的资料清单。
4.3.2 试验用药物
4.3.2.1 由申办方/CRO监查员、药物管理员、质量管理员三方共同完成试验药物交接,一般情况下需在启动会前交接完毕。若通过快递方式交接的,接收记录中需注明快递公司并保留快递单。
4.3.2.2 试验用药物运输过程需保存湿温度记录,常温与室温储存的药物同样需要运输过程的温湿度记录。若有特殊储存条件的药物建议采用冷链方式运送。
4.3.2.3 我院采取“机构药库+科室药物储存室”的管理模式,试验药物管理相关事宜可直接联系机构药库管理员。
机构药库管理员:吴巧稚
联系电话:025-89699088(外线)
药库地址:红宝石hbs最新网站hbs1231号楼负一楼机构药库
4.3.2.4 试验药物交接时,需同时提供以下文件:
l 药检合格报告
l 药物运输过程的温湿度记录
l 申办方药物交接单
l 药物运送的快递单(如适用)
4.3.3 试验用医疗器械(包括体外诊断试剂)
4.3.3.1 申办方/CRO监查员负责将试验用医疗器械运送至科室,与科室器械管理员完成交接手续,并签名确认。一般情况下需要在启动会前交接完毕。若通过快递方式交接的,接收记录中需注明快递公司并保留快递单。
4.3.3.2 试验用医疗器械运输过程中的保存条件参照说明书要求进行验收。
4.3.3.3 试验用医疗器械交接时,需同时提供以下文件:
l 自检报告和具有资质的检验机构出具的一年内的产品注册检验合格报告
l 医疗器械说明书
l 试验用医疗器械运输过程的温湿度记录
l 申办方医疗器械交接单
l 试验用医疗器械运送的快递单(如适用)
4.3 启动会
4.4.1 我院启动会由机构办主持召开,相关物资到位后,CRA与科室主要研究者协商启动会时间及地点,确定好后通知机构办。启动会参加人员至少应包括:研究者、参与试验人员、机构办工作人员、质量管理员、申办方/CRO代表、SMO代表等。
4.4.2 会议资料
l 临床试验方案、研究者手册
l 知情同意书、研究病历、病例报告表以及试验过程中用到的相关表格等至少备一份以便模拟试验流程。
l 培训 PPT,内容应包括:试验用药物/医疗器械简介及研究背景、试验步骤、 入排标准、知情同意过程、病例报告表的填写、评价方法、药物/医疗器械管理、AE/SAE的报告程序、试验的注意事项、监查计划等。
l 《临床试验方案启动和培训记录表》、《方案启动和培训签到表》、《临床试验分工授权表及签名样张》等表格,可以由申办方/CRO提供,也可由机构办提供。
4.4.3 主要研究者明确工作分工,并对试验相关人员进行授权。
4.4.4 研究人员模拟试验流程,就试验及过程进行讨论。
4.4.5 会议资料交科室/机构资料管理员归档,包括:相关表格、培训PPT、会议照片等。
5 项目实施
5.1 质量控制和质量管理
5.1.1 我院实行包括专业质控和机构办质控两个层面的二级质控,研究者对试验病例的可溯源性、规范性以及方案依从性负责,专业和机构办质控员负责临床试验的质量检查。
5.1.2 专业对每项临床试验明确专门的质控员,项目质控员不参与试验操作。项目质控员负责检查每一份研究病历和病例报告表,填写专业科室质控记录,并将质控检查问题及时向主要研究者报告。试验期间项目质控员每季度将质控检查结果汇总告知机构办质量管理员。
5.1.3 机构办定期对临床试验的管理和实施开展评审,评估存在问题,采取针对性改进措施,监督落实,确保临床试验质量管理的持续改进。
5.1.4 机构和专业主动接受来自申办方以及主管部门的监查、稽查和视察,以求不断提升临床试验质量。
5.2 SAE 报告
研究者获知SAE后立即向主要研究者和机构办报告,填写《SAE/SUSAR报告表》,并及时向申办方报告。
5.3 监查工作
监查员应严格按照法规要求开展监查工作。监查员在每次访视前必须通知机构办公室(发送访视确认函至机构邮箱),监查结束后原则上一周内将监查报告发送至机构邮箱,监查报告至少包括试验进度及存在问题。若在项目进行过程中更换监查员,需按前述4.1的要求,重新备案。
5.4 经费管理
5.4.1 经费立账流程
机构办接到财务科经费到账通知后,核实经费来源和经费归属,编制院内编号,填写“交费通知单”递交财务科,办理立项和入账手续。
5.4.2 经费报销流程
l 科室至机构办领取“临床试验经费本”,按照医院财务报销要求填写“红宝石hbs最新网站hbs123报销凭证”;
l 机构办根据项目试验方案、项目合同以及经费使用的相关规定,对报销票据进行审查及登记;
l 科室将机构办审查通过的报销单递交至财务科,由财务科审核票据的合法性和准确性;
l 财务科审核通过后,交由分管领导和院长审批,最后至财务科报销。
5.4.3 经费结题流程
所有受试者完成随访后,由申办方/CRO、主要研究者根据合同约定核实费用支出情况,申办方/CRO完成尾款支付。尾款支付成功后,科室按照合同条款提交费用结算清单,清单要求列出每个病例的受试者费用、受试者医疗开支、研究者观察费等,经主要研究者审核无误并签字后交至机构办公室。费用结算完毕后临床试验项目方可结题。
6 项目结束





6.1 项目结题
6.1.1 专业自查
临床试验结束前,各专业进行结题自查,针对发现问题采取解决措施,完成《临床试验结题自查表》。
6.1.2 资料交接
研究者按照《临床试验存档资料清单》顺序整理资料后,将审核签字确认的研究资料移交至机构办,机构办对研究资料进行终末质控,质控有问题资料退还至研究者修改,全部研究资料终末质控合格后存放于机构办资料室。
6.1.3 数据交接(适用于纸质CRF表)
临床试验费用结清后,机构办向申办方移交CRF表(第二联)。
6.1.4 数据答疑
l 对于数据记录和录入过程中出现的疑问,数据统计单位出具《数据答疑表》, 由监查员移交研究者进行确认。
l 研究者在答疑表中做出答疑,监查员可予以必要的协助。
l 经研究者签名确认的《数据答疑表》需在机构办保存一份副本。
6.1.5 分中心小结
所有受试者完成随访、研究者完成原始数据及文件的核查与数据答疑后,由主要研究者完成《分中心小结表》,签字确认后递交至机构办。
6.2 总结报告
6.2.1 撰写总结报告
统计分析报告完成后,由组长单位、申办方共同撰写总结报告初稿。
6.2.2 总结会
在召开试验项目总结会前,监查员需提前将会议邀请函及总结报告初稿等电子版资料,发送至机构办邮箱jshjgb@126.com,同时提交纸质版本。参会人员名单由机构办与科室负责人/主要研究者共同确定。
6.2.3 总结报告定稿
l 监查员将定稿的总结报告(电子版)同时发送至机构办和主要研究者的邮箱,各方审阅总结报告内容;
l 将定稿的总结报告(纸质版)递交给主要研究者,审定并签字确认;
l 将主要研究者签字确认的总结报告递交至机构办申请加盖机构公章;
l 总结报告一式多份,均需加盖骑缝章,盖章后需提供一份副本由机构办保存。
6.2.4 伦理结题申请
申办方需配合主要研究者,向伦理委员会提交结题申请。
7 说明
7.1 科室/申办方/CRO等应与机构办公室保持及时沟通,出现问题时应协调解决。
7.2 本工作指引所列内容和流程均为一般情况,仅供参考。个别特殊情况,以相互沟通结果为准。
7.3 本工作指引中未涉及到的事宜,请直接与机构办公室联系。